국내 개발 메르스 검사시약 첫 제조 허가
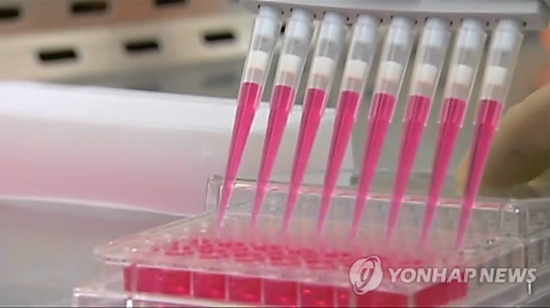
질병관리본부 국립보건연구원은 국내에서 개발된 메르스(MERS) 바이러스 검사시약이 처음으로 식품의약품안전처로부터 체외진단용 의료기기로 품목 제조허가를 취득했다고 30일 밝혔다. 국립보건연구원은 작년 메르스 유행 당시 연구용역사업으로 진단시약 개발을 추진했다. 허가받은 검사시약(PowerCheckTM MERS< upE & ORF1a> Real-time PCR kit)은 환자의 호흡기 검체에서 추출된 바이러스 유전물질(Viral RNA)을 이용해 메르스 바이러스의 감염 여부를 확인하는 제품이다. (연합)